Acetato de ulipristal
Recientemente se ha aprobado el uso del acetato de ulipristal como contragestativo de emergencia, que puede utilizarse hasta 120 horas después de una relación sexual no protegida, cuya comercialización para su uso clínico autorizó la Agencia Europea del Medicamento (EMEA) el 19 de marzo de 2009 [1].
El acetato de ulipristal, desarrollado por HRA Pharma (UK Limited, Kensal Green, London), contiene 30 µg de ulipristal acetato micronizado y se distribuye con el nombre comercial de EllaOne [2].
Composición química y acción farmacológica[editar | editar código]
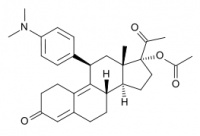
El Ulipristal, 17α-acetoxi-11α- (4-N,N-dimetilaminofenil)-19-norpregna-4,9-dieno-3,20-diona, también conocido como CDB-2914, VA2914, HRP-2000 y RTI-3021-012, es un derivado de la 19-norprogesterona, con una sustitución 11β-aril, similar a la mifepristona.
Desde un punto de vista farmacológico, el ulipristal acetato actúa como un antagonista de los receptores de la progesterona sin actividad agonista 8,9,10.
Eficacia clínica[editar | editar código]
Los estudios de eficacia clínica del ulipristal acetato se han centrado en su actividad anticonceptiva o contragestativa, generalmente comparándola con algún otro contraceptivo de emergencia, como parámetro de referencia.
Para evaluar su eficacia clínica se utiliza el índice o tasa de embarazos, entendiendo por tal el cociente entre el número de embarazos observados y el número total de mujeres introducidas en un determinado ensayo clínico. Este índice refleja la proporción de embarazos evitados por la administración del fármaco evaluado.
En cuanto a la eficacia clínica del acetato de ulipristal existen tres trabajos bien diseñados sobre el tema [3], [4] ,[5].
- En el primero de ellos, Creinin y col [3]llevan a cabo un ensayo clínico de fase II, aleatorio, doble ciego y placebo, que incluye 1672 mujeres de entre 18 y 44 años, dándoles 50 µg de ulipristal no micronizado o 750 µg de levonorgestrel, en dos dosis separadas 12 horas, administrado entre 0 y 72 horas después de la relación sexual.
Los resultados muestran que en el grupo de mujeres tratadas con CDB-2914 (Ulipristal), la tasa de embarazos fue del 0,9% (95% CI 0,2%-1,6%) y en el grupo control (levonorgestrel) del 1,7% (95% CI 0,8%-2,6%). - En el segundo trabajo, de Glasier y colaboradores [4], se utilizan 30 µg de ulipristal acetato micronizado en el grupo problema y 1500 µg de levonorgestrel en una sola dosis, en el grupo control.
En este trabajo se incluyen 1899 mujeres, distribuidas en dos grupos de 1696 y 203 mujeres. En el primer grupo todas recibieron el fármaco correspondiente antes de transcurridas 72 horas desde la relación sexual no protegida. De ellas 844 mujeres fueron incluidas en el grupo del ulipristal y 852 en el del levonorgestrel. La tasa de embarazos fue del 1,8% en el grupo del ulipristal (95% CI 1,0%-3,0%) y del 2,6% (95% CI 1,7%-3,9%) en el grupo del levonorgestrel. Al segundo grupo de 203 mujeres se les administró la píldora contragestativa entre las 72 y 120 horas después de la relación sexual no protegida. En este grupo se detectaron tres embarazos, todos ellos utilizando el levonorgestrel. Considerados estos datos globalmente, es decir, durante el periodo de 0 a 120 horas, la tasa de embarazos para el ulipristal acetato fue del 1,8% y de 2,6% para el levonorgestrel, aunque las diferencias observadas no fueron estadísticamente significativas, pero sí lo fueron las obtenidas en el grupo de mujeres que recibieron el contragestativo entre las 72 y 120 horas. - El tercer estudio, de Fine y col [5], es un ensayo clínico de fase III, multicéntrico y sin placebo, en el que se administró una única dosis de ulipristal acetato de 30µg micronizado, entre las 48 y las 120 horas después de la relación sexual no protegida a 1533 mujeres, de las que finalmente fueron evaluadas 1241.
La tasa global de embarazos para el conjunto del periodo de 48 a 120 horas fue del 2,1 % (95% CI 1,4%-3,1%), habiéndose observado 26 embarazos entre las 1241 mujeres, lo que en relación con el 5,5% de embarazos esperados [6], supone una eficacia preventiva global del 62%.
Efectos secundarios[editar | editar código]
Según los datos del informe elaborado por EMEA[7], los efectos secundarios constatados por el uso del ulipristal acetato, cuando se administran 30 µg micronizados, son leves o moderados y remiten espontáneamente. Los más frecuentes fueron, dolor de cabeza, náuseas y dolor abdominal, habiéndolos padecido alrededor del 10% de las usuarias. Sin embargo, en el trabajo de Glasier y Col [4], que incluye los efectos secundarios tanto del ulipristal acetato como del levonorgestrel, los porcentajes de efectos secundarios negativos son objetivamente superiores a los del informe EMEA, ya que detectaron:
- Dolor de cabeza, aproximadamente en el 19%.
- Dismenorrea y náuseas en el 17%.
- Fatiga, mareos y dolor abdominal aproximadamente en el 5%.
- Dolor de espalda en el 3%.
Mecanismo de acción contragestativo[editar | editar código]
Los primeros estudios sobre el mecanismo de acción contragestativo del ulipristal acetato se realizaron utilizando el producto conocido como CDB-2914. En el primero de ellos [8], el fármaco se administró en la fase preovulatoria, cuando el tamaño del folículo oscilaba entre 14 y16 mm. En todos los caso se produjo un retraso de la ovulación que fue mayor con las dosis más altas del fármaco, ovulando en este caso hasta 7 días después de su administración. Cuando se administro en la fase luteínica se pudo comprobar que inhibía la maduración endometrial.
En 2003, Passaro y colaboradores [9] evaluaron así mismo el efecto del CDB-2914, pero en este caso administrándolo en el sexto día de la fase luteínica, comprobando que se producía un sangrado endometrial prematuro, sin duda indicador de un efecto directo sobre el endometrio, acción similar a la producida por la mifepristona.
En un tercer trabajo, en el que se utilizó el VA-2914, Mutter y Col[10] encontraron objetivas modificaciones del endometrio que calificaron como “cambios endometriales asociados a los inhibidores selectivos de la progesterona”, en este caso el VA-2914.
También Ravet y Col [11], tras administrar durante 12 semanas dosis bajas de VA-2914, realizaron una biopsia endometrial a los seis u ocho días del pico de la LH, comprobando la existencia de una atrofia endometrial.
Finalmente, de los trabajos realizados con variantes farmacológicas del ulipristal acetato distintas de EllaOne, el último es el de Stratton y col [12], quienes comprueban que administrando el fármaco uno o dos días después del pico de la LH se produce una significativa reducción del grosor del endometrio en el grupo de mujeres que reciben el fármaco comparado con el grupo placebo. Menos frecuentemente observan atrofia endometrial y persistencia del endometrio proliferativo en la fase luteínica del ciclo, cuando se utilizan las dosis más altas de CDB-2914 (100 mg).
De todos los datos anteriormente referidos se deduce el objetivo efecto que el ulipristal acetato, en sus presentaciones CDB-2914 y VA-2914, tiene sobre el endometrio de la mujer que lo recibe, lo cual sin duda avala que en su mecanismo contragestativo juega un papel importante el efecto antiimplantatorio.
Ya en relación con el ulipristal acetato, en su presentación de EllaOne, la píldora de los cinco días después, en un trabajo [13] referido de forma específica al mecanismo por el cual previene los embarazos no deseados, trabajo elaborado utilizando los informes de la propia compañía que produce el fármaco, la HRA Pharma, de la Agencia Europea del Medicamento y el elaborado por el Real Colegio de Obstetras y Ginecólogos del Reino Unido, se constata que el ulipristal acetato, en un porcentaje que oscila entre el 50% y el 70% de las veces, actúa por un mecanismo antiimplantatorio.
En otros trabajos[14] en los que se ha evaluado la relación entre el efecto anovulatorio y antiimplantatorio, se ha visto que el primero disminuye rápidamente según el día en el que se tome la píldora y por tanto crece el efecto segundo.
En la tabla se evalúa el efecto contragestativo del fármaco atendiendo a dos parámetros, el día en que la mujer tiene la relación sexual con respecto al día de la ovulación y el tiempo que tarde en tomar el fármaco después de la relación sexual, observándose que, si la relación sexual se tiene 5 días antes de la ovulación y el fármaco se toma dentro de las primeras 24 horas después de ésta, el efecto anovulatorio, entendiendo por tal la inhibición o retraso de la ovulación, sería del 100%. Lo mismo ocurre si se toma a las 48 horas; pero disminuye al 78,6%, si se toma a las 72 horas y al 8,3%, si se toma a las 96 horas. Por tanto el efecto anovulatorio global, cuando la relación sexual se tiene 5 días antes de la ovulación y el fármaco se toma entre las 0 y 96 horas después de ésta, sería de 57,4%. Siguiendo el mismo razonamiento, el efecto global anovulatorio cuando se toma hasta 48 horas después de la relación sexual sería del 37,4%, si es a las 72 horas es de 17,4% y si se toma a las 96 horas del 1,7%, actuando por un efecto antiimplantorio, en todos los demás casos.
En una revisión bibliográfica de 2016[15] se concluye que aunque fue un medicamento pensado para trabajar por la prevención de la fertilización. Investigaciones recientes han puesto en duda esto. En esta revisión de la bibliografía se ve que se podría prevenir la ovulación en sólo el 15 por ciento o menos de los casos. El fármaco no tiene la capacidad de alterar la función del esperma y una capacidad limitada para suprimir la ovulación. Además, los datos sugieren que cuando se administra antes de la ovulación, puede también tener un mecanismo de acción después de la fertilización.
Aspecto ético[editar | editar código]
El aspecto ético del uso del acetato de ulipristal depende de dos cuestiones:
- Anovulatorio y antiimplatatorio: que se considere su aspecto anovulatorio o su aspecto antiimplantatorio. En el primer caso no se produciría la fecundación por lo que para evitar el embarazo no deseado no habría que destruir ningún embrión humano. En cambio, si ésta píldora contraceptiva actúa por un mecanismo antiimplantatorio, estaría consiguiendo su objetivo antiembarazo destruyendo la vida de un embrión humano que ya ha iniciado su andadura vital. Por esta razón es fundamental determinar el mecanismo de acción del ulipristal acetato para llevar a cabo un juicio ético sobre su uso.
- En ocasiones, se afirma de una manera absoluta que la píldora de los 5 días después, el ulipristal acetato, actúa únicamente impidiendo la ovulación y consiguientemente por un mecanismo antiimplantatorio. Así, por ejemplo, el grupo de Croxatto, se muestran tendente a destacar la actividad anovulatoria de los fármacos utilizados en la contracepción de emergencia, tanto del levonorgestrel como del ulipristal acetato, en detrimento de su acción antiimplantatoria. En este sentido parece de interés señalar que en uno de sus más significados trabajos, el publicado en 2004[16], los autores manifiestan que “el levonorgestrel puede alterar el proceso ovulatorio en el 93% de los ciclos tratados, cuando el diámetro de los folículos oscila entre 12 y 17 mm”.
- Sin embargo, en su último trabajo, el publicado en 2010[17], taxativamente afirman, al evaluar el mecanismo de acción del ulipristal acetato, que “los actuales métodos de contracepción de emergencia son inefectivos para prevenir la ruptura folicular cuando se administran en la fase preovulatoria avanzada, cuando el folículo es mayor de 18 mm”, es decir basta que el folículo pase de 17 a 18mm, para que el mecanismo contragestativo pase de ser en el 93% de los casos anovulatorio a ser antiimplantatorio.
- Pero además, también en dicho trabajo se comenta que, “la ruptura folicular ocurre en la mayoría de los ciclos, pero más tarde de lo esperado”, lo que sin duda podría indicar que en caso de una relación sexual tardía se podría producir la fecundación, por lo que si en este caso se impidiera el embarazo, siempre lo haría por un mecanismo antimplantatorio. Además, en este trabajo, se afirma “ que un folículo intacto está todavía presente en el quinto día después de la administración del ulipristal acetato en casi el 60% de las mujeres que lo toman (concretamente en el 57%) y en ninguna del grupo placebo. Lo que significa que en aproximadamente el 43% de las veces la acción del fármaco no afecta a la ovulación y consecuentemente para impedir el embarazo no deseado tiene que actuar evitando que el embrión ya generado se implante en su madre.
- Valor de la vida humana incipiente. La segunda cuestión es la valoración ética que se haga de la vida del embrión humanos antes de su implantación. Si se le niega valor como ser humano, y por tanto dignidad, o se reconoce que se encuentra ante un individuo humano, y por tanto con la dignidad que impide que sea destruido.
- El 25 de junio de 2015 el Tribunal Constitucional español ha reconocido el derecho a la objeción de conciencia de los farmacéuticos que se abstengan de vender la píldora del día después, mientras que no se reconoce para la no dispensación de preservativos[18]
Referencias[editar | editar código]
- ↑ Committee for Medicinal Product for Human Use(CHMP). Summary of Positive Opinion for EllaOne Consultado 04.08.2009
- ↑ EllaOne 30 mg. HRA Pharma UK daunted. Summary of Product Charcteristics last update on the emc: 18-IX-2009 Consultado 22 de agosto 2011
- ↑ 3,0 3,1 Creining MD et al. Progesterone receptor modulator for emergency contraception contraception: A randomized controlled trial. Obstet Gynecol. 108(5); 1089-1097, 2006
- ↑ 4,0 4,1 4,2 Glasier AF, Cameron ST et al. Ulipristal acetate versus levonorgestrel for emergency contraception: a randomized non inferiority trial and meta-analysis. Lancet. 375; 555-562, 2010.
- ↑ 5,0 5,1 Fine P et al. Ulipristal acetate taken 48-120 hours after intercourse for emergency contraception. Obstetrics and Gynecology. 115; 257-263, 2010.
- ↑ Trussell J, Ellertson C et al. Estimating the effectiveness of the emergency contraceptive pills. Contraception. 67; 259-265, 2003
- ↑ European Medicine Agency. Evaluation of Medicines for Human Use. Doc. Ref: EMEA/261787/2009 Consultado 17.07.2010
- ↑ Stratton P, Hartog B et al. A single mid-follicular dose of CDB-2914, a new antiprogestine, inhibits folliculogenesis and endometrial differentiation in normally cycling women. Hum. Reprod. 15; 1092-1099, 2000
- ↑ Passaro MD, Piquion J. Luteal phase dose-response relationships of the antiprogestin CDB-2914 in normally cycling women. Human Reproduction. 18(9); 1820-1827, 2003
- ↑ Mutter GL, Bergeron C et al. The spectrum of endometrial pathology induced by progesterone receptor modulators. Modern pathology. 21; 591-598, 2008.
- ↑ Ravet S, Munaut C et al. Persistence of an intact endometrial matrix and vessels structure in women exposed to VA-2914, a selective Progesterone receptor modulator. J Clin Endocrinol Metab. 93(11); 4525-4531, 2008
- ↑ Stratton O, Levens ED et al. Endometrial effects of a single luteal dose of the selective progesterone
- ↑ Aznar J. Ulipristal acetate. A new emergency contraceptive. Ethical aspects of its use. Medicina e Morale. 1; 15-21, 2010
- ↑ Croxatto H, Brache V et al. Pituitary ovarian function following the standard levonorgestrel emergency contraceptive dose or a single 0.75 mg dose given on the days preceding ovulation. Contraception. 70; 442-450, 2004.Brache V, Cochon L et al. Inmediate pre-ovulatory administration of 30 mg. Ulipristal acetate significantly delays follicular rupture. Hum. Reprod. 0; 1-9, 2010.
- ↑ Rebeca Peck, Walter Rella, Julio Tudela, Justo Aznar and Bruno Mozzanegas, Does levonorgestrel emergency contraceptive have a post-fertilization effect? A review of its mechanism of action, The Linacre Quaterly, 83, 1,35-51,2016 Consultado 7 de mayo 2016
- ↑ Croxatto H, Brache V et al. Pituitary ovarian function following the standard levonorgestrel emergency contraceptive dose or a single 0.75 mg dose given on the days preceding ovulation. Contraception. 70; 442-450, 2004
- ↑ Brache V, Cochon L et al. Inmediate pre-ovulatory administration of 30 mg. Ulipristal acetate significantly delays follicular rupture. Hum. Reprod. 0; 1-9, 2010.
- ↑ «Sentencia 145/2015, de 25 de junio de 2015». BOE (182): 66654. 2015. Consultado el 29 de junio de 2016.
Bibliografía[editar | editar código]
- Justo Aznar, Contracepción de emergencia Consultado el 22 de agosto 2011
- Página de la empresa farmaceútica HRA-Pharma
- Precio de ellaOne -España-
- Justo Aznar, Ulipristal acetato, un contraceptivo de emergencia ( EllaOne) Consultado el 23 de agosto de 2011